В настоящее время в строительстве и различных отраслях промышленности широко применяются синтетические смолы, получаемые в результате реакций поликонденсации или полимеризации. Наиболее широко они используются в качестве связующих для получения композиционных материалов, клеев и в лакокрасочной промышленности. Основными преимуществами применения синтетических смол являются их высокая адгезия к большинству материалов и водостойкость, а также механическая прочность, химическая и термическая устойчивости [2, 4, 8].
При этом в чистом виде синтетические смолы практически не используются, а применяются в качестве основы композиций, в состав которых входят различные добавки такие как наполнители, разбавители, загустители, отвердители и др.
Введение добавок позволяет в широких пределах регулировать технологические свойства композиций и эксплуатационные свойства получаемых из них изделий. Однако во многом свойства композиции определяются свойствами синтетической смолы. От выбора смолы также зависит выбор технологии и параметров формования изделий из композиции.
К наиболее широко применяемым в настоящее время синтетическим смолам относятся карбомидные, алкидные, эпоксидные, полиамидные и фенолоальдегидные (преимущественно фенолоформальдегидные) [2, 4].
Общая характеристика фенолоформальдегидных смол ФФС [–C6H3(OH) –CH2–]n являются жидкими или твердыми олигомерными продуктами реакции поликонденсации фенола C6H5OH или его гомологов (крезолов CH3–C6H5–OH и ксиленолов (CH3)2–C6H5–OH) с формальдегидом (метаналем Н2–С=О) в присутствии катализаторов кислотного (соляная HCl, серная H2SO4, щавелевая Н2С2О4 и другие кислоты) и щелочного (аммиак NH3, гидрат аммиака NH4OH гидроксид натрия NaOH, гидроксид бария Ba(OH)2) типа.
Формальдегид обычно применяют в виде водного раствора, стабилизированного метанолом, который называется формалином CH2O • Н2О • СН3OН. В ряде случаев фенол заменяют на замещенные фенолы или резорцин (С6Н4(ОН)2), а формальдегид частично или полностью замещают на фурфурол С5Н4О2 или на продукт полимеризации формальдегида – параформ OH(CH2O)nH, где n = 8 – 100 [12].
Роль реакционноспособных функциональных групп в этих соединениях играют:
В феноле – три С-Н-связи в двух орто- и пара-положениях (легче идет замещение в двух орто-положениях);
В формальдегиде – двойная связь С=О, способная к присоединению по атомам С и О.
В зависимости от природы в соотношения компонентов, а также от применяемого катализатора фенолоформальдегидные смолы делят на два вида: термопластичные или новолачные смолы и термореактивные или резольные.
Процесс образования фенолоальдегидных смол весьма сложен. Ниже приведены реакции образования фенолоформальдегидных смол, установленные на основании работ Кебнера и Ваншейдта и являющиеся в настоящее время общепризнанными [2].
Характеристика новолачных смол
Новолачные смолы (НС) – преимущественно линейные олигомеры, в молекулах которых фенольные ядра соединены метиленовыми мостиками –СН2–. Для получения новолачных смол необходимо проводить реакцию поликонденсации фенола и формальдегида при избытке фенола (отношение фенола к альдегиду в молях 6 : 5 или 7 : 6) и в присутствии кислых катализаторов.
При этом на первой стадии реакции будут образовываться п- и о-монооксибензиловые спирты [2]:
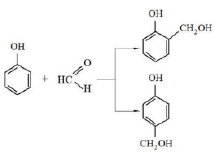
В кислой среде фенолоспирты быстро реагируют (конденсируются) с фенолом и образуют дигидроксидифенилметаны, например [2]:
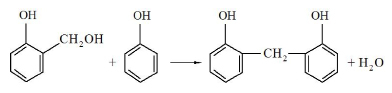
Образовавшиеся дигидроксидифенилметаны взаимодействуют с формальдегидом или фенолоспиртами. Дальнейший рост цепи происходит за счет последовательного присоединения формальдегида и конденсации.
Общее уравнение поликонденсации в кислой среде, приводящее к образованию НС, имеет вид [2]:
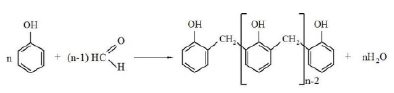
где n ≈ 10.
При обычных условиях новолачной конденсации присоединение формальдегида к фенольному ядру происходит в основном в пара-положение, и приведенная выше формула не отражает истинного строения смолы. Ортоноволаки, т. е. фенолоформальдегидные олигомеры с присоединением только в орто-положение, получаются лишь при специальных методах поликонденсации. Они представляют значительный интерес благодаря регулярному строению и возможности получения сравнительно высокомолекулярных соединений.
Молекулы новолачной смолы не способны вступать в реакцию поликонденсации между собой и не образуют пространственных структур.
Отверждение новолачных смол
Новолачные смолы представляют собой термопластичные полимеры, которые при нагревании размягчаются и даже плавятся, а при охлаждении затвердевают. Причём этот процесс можно проводить множество раз.
Новолачные смолы могут быть переведены в неплавкое и нерастворимое состояние путем обработки их различными отвердителями: формальдегидом, параформом или чаще всего гексаметилентетрамином (уротропин) С6Н12N4 [2]:
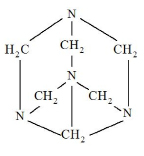
Уротропин добавляют в количестве 6 – 14 % и нагревают смесь при температуре 150 – 200оС. Измельченная смесь новолачной смолы с гексаметилентетрамином (уротропином) называется пульвербакелит [9].
При нагревании происходит разложение уротропина с образованием диметилениминовых (I) и триметиленаминовых (II) мостиков между молекулами смолы [2]:
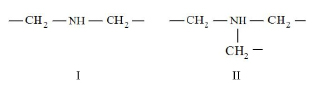
Эти мостики затем распадаются с выделением аммиака и других азотсодержащих соединений, а между молекулами смолы образуются метиленовые мостики —СН2— и термостабильные связи —СН=N—СН2—.
Новолачные смолы при нагревании с уротропином проходят те же три стадии отверждения, что и резольные.
Свойства новолачных смол
В зависимости от технологии получения новолачные смолы представляют собой твердые хрупкие стеклообразные вещества в виде кусков, чешуек или гранул цветом от светло-жёлтого до тёмно-красного (рис. 1).

Рис. 1. Внешний вид новолачных смол
Таблица 1
Свойства новолачных смол в присутствии 10 % гексаметилентетрамина (уротропина)
|
Молекулярная масса, г/моль |
Плотность, кг/м3 |
Содержание свободного фенола, % |
Температура каплепадения*, оС |
Время желатинизации** при 150оС, с |
|
450 – 800 |
1200 – 1220 |
1 – 7 |
90 – 130 |
40 |
Примечания: *Температура каплепадения – температура, при которой смола начинает принимать жидкую форму и спадает в форме капель или выплывает из измерительного сосуда под действием силы тяжести. **Время желатинизации – время, в течении которого смола полимеризуется и переходит в твердое, неплавкое и нерастворимое состояние. В течении этого времени смола остаётся жидкой, пригодной для обработки и применения.
Новолачные смолы хорошо растворимы в спиртах, кетонах, сложных эфирах, фенолах и водных растворах щелочей. В воде новолачные смолы набухают и размягчаются, а в отсутствии влаги стабильны при хранении.
Основные свойства новолачных смол, выпускаемых промышленностью (марок СФ) представлены в табл. 1 [7].
Характеристика резольных смол
Резольные смолы (РС), называемые также бакелитами – смесь линейных и разветвлённых олигомеров, содержащих большое число метилольных групп –СН2ОН, способных к дальнейшим превращениям. Для получения резольных смол необходимо проводить реакцию поликонденсации фенола и формальдегида при избытке формальдегида (отношение альдегида к фенолу в молях 6 : 5 или 7 : 6) и в присутствии основных катализаторов.
При этом на первой стадии реакции поликонденсации будут получаться моно-, ди- и триметилольные производные фенола (фенолоспирты) [2]:
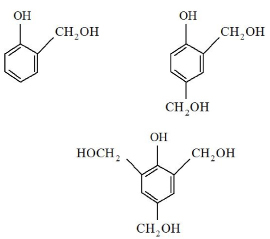
При температурах выше 70°С фенолоспирты взаимодействуют друг с другом с образованием двух- и трехъядерных соединений [2]:
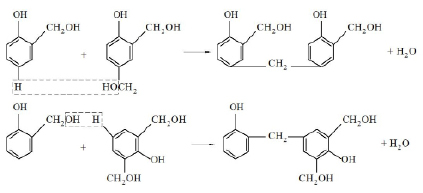
Образовавшиеся димеры могут реагировать с моноспиртами или друг с другом, образуя олигомеры с более высокой степенью поликонденсации, например [2]:
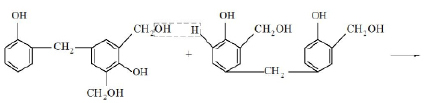
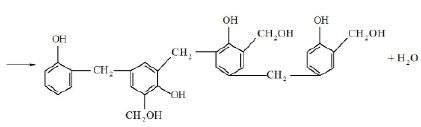
Общее уравнение поликонденсации в этом случае может быть представлено следующим образом [2]:
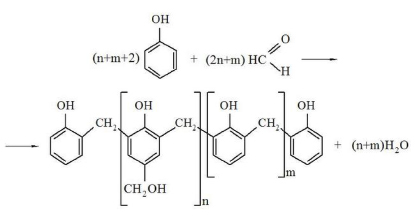
где m = 4 – 10, n = 2 – 5.
Полученная в результате подобной реакции поликонденсации смола называется резол.
Резольные смолы в некоторых случаях могут содержать также диметиленэфирные группы —СН2—О—СН2—, за счет чего из них при нагревании выделяется формальдегид.
Отверждение резольных смол
Резольные смолы представляют собой термореактивные полимеры, которые при нагревании подвергаются необратимому химическому разрушению без плавления. При этом происходит необратимое изменение свойств в результате сшивания молекулярных цепей поперечными связями. Смола отверждается и переходит из расплавленного состояния в твердое. Температура отверждения может быть, как высокой (80–160оС [9]) при горячем отверждении, так и низкой – при холодном отверждении. Отверждение происходит за счет взаимодействия функциональных групп самого материала или при помощи отвердителей, аналогичных применяемым для новолачных смол.
Резольные смолы отверждаются также при длительном хранении даже при обычной температуре.
Различают три стадии конденсации или три типа резольных смол [8, 9]:
Стадия А (резол) – смесь низкомолекулярных соединений продуктов реакции поликонденсации;
Стадия В (резитол) – смесь резольной смолы и высокомолекулярных неплавких и нерастворимых соединений.
Стадия С (резит) – смола, состоящая в основном из трехмерных высокомолекулярных соединений.
Эти превращения происходят в результате конденсации метилольных групп с подвижными атомами водорода в орто- и пара-положениях фенильного ядра [2]:
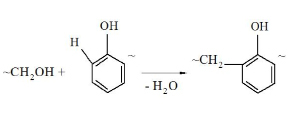
А также взаимодействия метилольных групп между собой [2]:
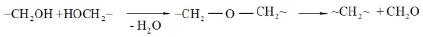
Строение резитов можно упрощенно представить следующим образом [2]:
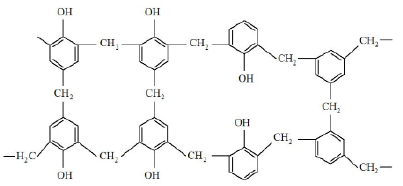
Отверждение резольных смол может идти и на холоду в присутствии кислот (соляной, фосфорной, п-толуолсульфокислоты и др.). Отвержденные в присутствии нефтяных сульфокислот RSO2OH (где R – углеводородный радикал) резиты называются карболитами, а в присутствии молочной кислоты С3Н6О3 – неолейкоритами.
При нагревании отверждение резольных смол ускоряется при добавке окислов щелочноземельных металлов: СаО, МgО, ВаО.
Свойства резольных смол
В начальном состоянии (стадия А) резольные смолы разделяются на твердые и жидкие. Твердые («сухие смолы») представляют собой твердые хрупкие вещества от светло-желтого до красноватого цвета в зависимости от применяемого катализатора и по внешнему виду мало отличаются от новолачных смол (см. рис. 1). Резольные смолы содержат большее количество свободного фенола, чем новолачные смолы, что приводит к снижению их температуры плавления. Резольные смолы как и новолачные растворяются в спиртах, кетонах, сложных эфирах, фенолах, водных растворах щелочей, а также набухают в воде.
Основные свойства твердых резолов, выпускаемых промышленностью (марок ИФ) представлены в табл. 2 [7].
Таблица 2
Свойства твердых резольных смол
|
Молекулярная масса, г/моль |
Плотность, кг/м3 |
Содержание свободного фенола, % |
Температура каплепадения, оС |
Время желатинизации при 150оС, с |
|
400 – 1000 |
1250 – 1270 |
5 – 12 |
70 – 110 |
60 – 120 |
Жидкие смолы представляют собой коллоидный раствор смолы в воде (рис. 2), получаемый в присутствии аммиачного или аммиачно-бариевого катализатора, и подразделяются на жидкие бакелиты и водоэмульсионные смолы.
Основные свойства жидких резолов, выпускаемых промышленностью (марок БЖ и ОФ) представлены в табл. 3 [7].

Рис. 2. Внешний вид жидких резольных смол
Таблица 3
Свойства жидких резольных смол
|
Марка |
Плотность, кг/м3 |
Вязкость, Па•с |
Содержание свободного фенола, % |
Содержание воды, % |
Время желатинизации при 150°С, с |
|
БЖ |
1190 – 1230 |
0,5 – 3 |
8 – 16 |
15 – 19 |
60 – 240 |
|
ОФ |
1130 – 1190 |
0,5 – 1,8 |
15 |
20 – 35 |
100 – 150 |
При нагревании или длительном хранении резол переходит в стадию В (резитол), а затем в стадию С (резит). Резитол нерастворим в растворителях, а только набухает в них, не плавится, но размягчается при нагревании.
Резит представляет собой твердое вещество цветом от светло-желтого до вишневого или коричневого. Резит не плавится и не размягчается при нагревании, нерастворим и не набухает в растворителях.
Основные свойства резитов, получаемых при отверждении резольных смол представлены в табл. 4 [7].
Таблица 4
Свойства резитов
|
Показатель |
Величина |
|
Плотность |
1250 – 1380 кг/м3 |
|
Разрушаемость от температуры |
240 – 260оС |
|
Водопоглощение через 24 часа |
0,05 – 0,2 % |
|
Предел прочности: – при растяжении – при сжатии – при статическом изгибе |
(42 – 67)•106 Па (8 – 15)•107 Па (8 – 12)•107 Па |
|
Твердость по Бринеллю |
10 – 50 |
|
Удельное электрическое сопротивление |
1•1012 – 5•1014 Па |
|
Электрическая прочность |
10 – 14 кВ/мм |
|
Диэлектрическая проницаемость при 50 Гц |
0,05 – 0,1 |
|
Дугостойкость |
Очень низкая |
|
Стойкость против слабых кислот |
Очень хорошая |
|
Стойкость против щелочей |
Разрушается |
Модифицирующие добавки для ФФС
Для направленного изменения свойств фенолоформальдегидных смол используют метод химической модификации. Для этого в реакцию при их получении вводят компоненты, способные взаимодействовать с фенолом и формальдегидом.
В первую очередь это отвердители, которые были рассмотрены ранее. В качестве ускорителей отверждения фенолформальдегидных смол применяют сульфаты, фосфаты и хлориды аммония в количестве 0,1–5 % [3].
Возможно применение смеси резольных и новолачных смол. При этом получаются менее жесткие материалы с лучшими адгезионными свойствами.
При введении анилина C6H5NH2 повышаются диэлектрические свойства и водостойкость, при введении карбамида CH4N2O – светостойкость, при введении фурилового спирта C4H3OCH2OH – химическая стойкость. Для улучшения стойкости к щелочам смолы модифицируют фтористыми соединениями бора или наполняют графитом или углем, а также добавляют до 20 % дихлорпропанола.
Для придания способности растворяться в неполярных растворителях и совмещаться с растительными маслами фенолоформальдегидные смолы модифицируют канифолью C19H29COOH, трет-бутиловым спиртом (CH3)3COH; смолы этого типа широко используют в качестве основы для фенолоальдегидных лаков.
Фенолоформальдегидные смолы совмещают с др. олигомерами и полимерами, например с полиамидами – для придания более высокой тепло- и водостойкости, эластичности, адгезионных свойств; с поливинилхлоридом – для улучшения водо- и химстойкости; с нитрильными каучуками – для повышения ударной прочности и вибростойкости, с поливинилбутиралем – для улучшения адгезии (такие смолы – основа клеев типа БФ). Для снижения хрупкости и внутренних напряжений применяют реакционноспособные каучуки (тиокол, фторлон).
Фенолоформальдегидные смолы используют для модификации эпоксидных смол с целью придания последним более высокой термо-, кислото- и щёлочестойкости. Возможна и модификация фенолоформальдегидных смол эпоксидными в сочетании с уротропином для улучшения адгезионных свойств, увеличения прочности и термостойкости изделий.
В последнее время фенолоформальдегидные смолы часто модифицируют меламином C3H6N6, получая меламинофенолоформальдегидные смолы.
Технология получения ФФС и композиций на их основе
Основными стадиями технологического процесса производства ФФС и композиций на их основе являются приготовление реакционной смеси, поликонденсация и сушка [11].
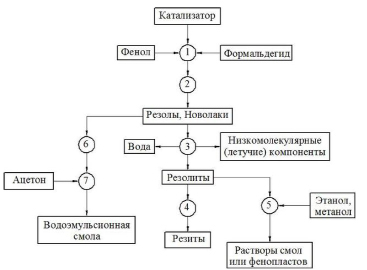
Рис. 3. Блок-схема технологического процесса производства ФФС и композиций на ее основе: 1– перемешивание в герметическом вакуумном реакторе с одновременным нагревом; 2 – поликонденсация в трубчатом холодильнике, сбор дистиллята и отвод в общую емкость (стадия А); 3 – обезвоживание и удаление низкомолекулярных (летучих) компонентов (стадия В); 4 – затвердевание в холодильном агрегате (стадия С); 5 – получение растворов; 6 – охлаждение до заданной вязкости и отделение надсмольной воды в отстойнике; 7 – сушка под вакуумом и разбавление растворителем
Приготовление реакционной смеси заключается в плавлении фенола и получении водных растворов катализатора. Реакционную смесь готовят либо в алюминиевых смесителях, либо непосредственно в реакторе. Состав реакционной смеси и технологические режимы производства зависят от вида получаемой смолы (НС или РС), функциональности и реакционной способности фенольного сырья, рН реакционной среды применяемого катализатора и вводимых добавок [9].
Производство новолачных смол и лаков
В производстве новолачных смол в качестве катализатора применяют соляную, реже щавелевую кислоту. Преимуществом соляной кислоты является высокая каталитическая активность и летучесть. Щавелевая кислота – менее активный катализатор, чем соляная кислота, однако процесс поликонденсации в ее присутствии легче управляем, а смолы получаются более светлыми и светостойкими. Каталитическое действие на процесс поликонденсации оказывает также муравьиная кислота, всегда присутствующая в формалине.
Обычно для производства новолачной смолы применяются следующие соотношения компонентов, (мас. ч.) [2]: фенол = 100; соляная кислота (в перерасчёте на НС1) = 0,3; формалин (в пересчете на формальдегид) = 27,4. Формалин представляет собой водный раствор, содержащий 37 – 40 % формальдегида и 6 – 15 % метилового спирта в качестве стабилизатора.
При периодическом методе получения НС (рис. 4) поликонденсацию и сушку проводят в одном реакторе. Для проведения поликонденсации смесь фенола и формальдегида загружают в реактор, снабженный теплообменной рубашкой и мешалкой якорного типа. Одновременно подают половину требуемого количества соляной кислоты (катализатор добавляется частями во избежание слишком бурного течения реакции). Реакционную смесь перемешивают в течении 10 минут и отбирают пробу для определения рН. Если рН находится в пределах 1,6—2,2 в рубашку реактора подают пар и нагревают реакционную смесь до 70 – 75°С. Дальнейший подъем температуры происходит за счёт теплового эффекта реакции [3].
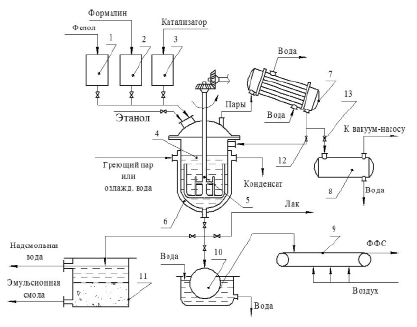
Рис. 4. Технологическая схема получения ФФС периодическим способом: 1 – 3 – мерники; 4 – реактор; 5 – якорная мешалка; 6 – теплообменная рубашка; 7 – холодильник-конденсатор; 8 – сборник конденсата; 9 – транспортер; 10 – охлаждающий барабан; 11 – отстойник; 12 – кран для подачи конденсата в реактор; 13 – кран для отвода воды и летучих компонентов из реактора
При достижении температуры смеси 90°С прекращают перемешивание и для предотвращения бурного кипения в рубашку подают охлаждающую воду, подачу которой прекращают после установления равномерного кипения. В этот момент вновь включают мешалку, добавляют вторую половину от общего количества соляной кислоты, а спустя 10–15 минут возобновляют подачу пара в рубашку реактора. Образующиеся в процессе кипения пары воды и формальдегида попадают в холодильник-конденсатор, из которого образующийся водный раствор вновь поступает в реактор.
Если вместо соляной кислоты применяется щавелевая, то ее загружают в количестве 1 % от массы фенола в виде водного 50 %-го раствора и в один прием, так как процесс протекает не столь интенсивно, как в присутствии соляной кислоты.
Поликонденсацию заканчивают, когда плотность образующейся эмульсии достигнет 1170 – 1200 кг/м3 в зависимости от природы фенольного сырья. Кроме плотности у получаемой смолы определяют способность к гелеообразованию путем нагрева до 200°С. В общей сложности длительность процесса составляет 1,5–2 часа.
По окончании реакции смесь в реакторе расслаивается: смола собирается внизу, а вода, выделившаяся при реакции и внесенная с формальдегидом, образует верхний слой. После этого начинают стадию сушки смолы. Воду и летучие вещества отгоняют, создавая в аппарате вакуум и используя конденсатор для их отвода в сборник конденсата. Во избежание переброса смолы в холодильник вакуум увеличивают постепенно. Температуру смолы к концу сушки постепенно повышают до 135–140°С. После завершения сушки следует выдержка при повышенной температуре (термообработка). Конец сушки и термообработки определяют по температуре каплепадения смолы, которая должна быть в пределах 95–105°С.
В готовую смолу вводят смазку (для некоторых видов пресс-порошков), перемешивают в течение 15–20 мин и сливают на охлаждающий барабан. Смола измельчается, попадает на обдуваемый воздухом транспортер, где охлаждается окончательно, после чего ее затаривают в бумажные мешки [2, 3].
Для получения лака высушенную смолу растворяют в этиловом спирте, который по окончании процесса сушки заливают непосредственно в реактор. Перед растворением прекращают подачу пара в рубашку и холодильник переключают на обратный. Нередко проводят совместную конденсацию формальдегида с фенолом и анилином. Полученные таким образом смолы являются связующими для пресс-порошков, из которых получают изделия с повышенными диэлектрическими свойствами. Отрицательное свойство анилинофенолоформальдегидных смол – их способность к самовозгоранию в процессе изготовления и при сливе.
Получение НС непрерывным способом (см. рис. 7) проводят в колонных аппаратах, работающих по принципу «идеального» смешения [2] и состоящих из трех или четырех секций, называемых царгами. Смесь фенола, формалина и части соляной кислоты готовят в отдельном смесителе и подают в верхнюю царгу, где она вновь перемешивается. После этого частично прореагировавшая смесь по переточной трубе переходит из верхней части царги в нижнюю часть следующей царги, последовательно проходя все секции аппарата. При этом в каждую царгу подается дополнительная порция соляной кислоты и происходит перемешивание смеси. Процесс проводят при температуре кипения смеси, равной 98–100оС [2, 3].
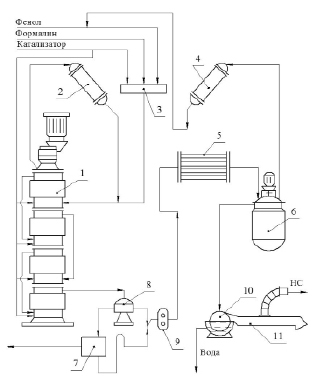
Рис. 5. Технологическая схема получения ФФС непрерывным способом: 1 – колонный реактор; 2,4 – холодильники; 3 – смеситель; 5 – сушильный аппарат (теплообменник); 6 – смолоприемник; 7 – отстойник; 8 – флорентийский сосуд; 9 – шестеренчатый сосуд; 10 – охлаждающий барабан; 11 – транспортер
Водно-смоляная эмульсия из нижней царги поступает для разделения в сепаратор, представляющий собой флорентийский сосуд. Водная часть из верхней части сепаратора подается в отстойник, а затем на дальнейшую очистку, а смоляную часть из сепаратора и отстойника шестеренчатым насосом перекачивается в трубное пространство теплообменника, в межтрубное пространство которого подается греющий пар под давлением 2,5 МПа. Смола в виде тонкой пленки движется по поверхности трубок теплообменника, нагреваясь до температуры 140–160оС. Полученная смесь смолы и летучих веществ попадает в смолоприемник – стандартизатор. Здесь летучие вещества удаляются из смолы и через верхнюю часть аппарата отводятся для последующей конденсации и подачи в смеситель для исходной реакционной смеси.
Горячая смола из смолоприемника сливается на барабан, который изнутри и снаружи охлаждается водой. В результате получается тонкая пленка смолы, которая подается на движущийся транспортер, где происходит окончательное охлаждение и испарение воды. Готовая смола может затариваться в мешки или отправляться на смешивание с добавками для получения различных композиций.
Производство резольных смол и лаков
В производстве резольных смол в качестве катализатора в основном применяют водный раствор аммиака. При большем избытке формальдегида роль катализаторов могут выполнять NаОН, КОН или Ва(ОН)2.
Обычно резольную смолу получают при следующих соотношениях компонентов, (мас.ч.) [2]: фенол = 100; аммиак (в виде водного раствора) = 1 – 1,5; формальдегид = 37.
Технологическая схема получения резольных смол в значительной степени аналогична схеме для получения новолачных смол (см. рисунки 6 и 7), однако есть и некоторые отличия. Так как тепловой эффект реакций получения резольных смол значительно меньше, чем при синтезе новолачных смол, катализатор вводится в реакционную смесь в один прием. Готовность смолы определяется путем определения ее вязкости и показателя преломления.
Сушку смолы начинают под вакуумом (93 кПа) при температуре 80°С с постепенным повышением давления и температуры (до 90–100°С) к концу процесса [2, 9]. Контроль сушки проводят путем определения времени гелеобразования смолы при 150°С.
При получении резольных смол важно не превышать температуру и строго выдерживать время, так как при несоблюдении температурно-временного режима возможно начало гелеобразования смолы в реакторе. Чтобы избежать гелеобразования высушенной смолы проводят ее быстрое охлаждение сразу после слива из реактора. Для этого ее сливают в вагоны-холодильники, представляющие собой тележки с вертикальными полыми металлическими плитами. Смолу сливают таким образом, чтобы в полостях соседних плит находилась охлаждающая вода.
Лаки и анилинофенолоформальдегидные смолы на основе резола получают таким же образом как и композиции на основе новолачных смол.
Производство эмульсионных резольных смол
Эмульсионные резольные смолы получают из смеси фенола или крезола с формалином в присутствии катализатора, в качестве которого чаще всего применяют Ва(ОН)2. Реакционную смесь нагревают в реакторе до 50–60°С, после чего она разогревается за счет теплового эффекта реакции. Температура смеси поддерживается в интервале 70–80°С и в случае перегрева в рубашку реактора подают охлаждающую воду. Синтез заканчивают, когда вязкость смолы при 20°С достигнет значений 0,16–0,2 Па•с [2, 9].
После этого реакционную смесь охлаждают до 30–45 °С [11], а затем подают в отстойник для отделения верхней водной части или проводят подсушку смолы под вакуумом до вязкости 0,4 Па•с с последующим разбавлением небольшим количеством ацетона. Стоит учитывать, что возможна дальнейшая самопроизвольная поликонденсация полученной эмульсионной смолы, для исключения которой ее хранят в охлаждаемых емкостях.
При производстве эмульсионных смол для получения пресс-материалов с длинноволокнистым наполнителем в качестве катализатора применяют NaOH. При этом время приготовления смолы составляет 100 минут с последующим охлаждением при температуре 70–80°С [11] путем подачи охлаждающей воды в рубашку реактора. После достижения смолой вязкости в пределах 0,02–0,15 Па•с [9] ее охлаждают до 30–35°С, отделяют от воды в отстойнике и переливают в охлаждаемый сборник. Готовая смола содержит до 20 % свободного фенола и 20–35 % воды [2].
Производство фенолоспиртов и фенолоформальдегидных концентратов
Фенолоспирты являются промежуточными продуктами получения резольных смол и отличаются высокой стабильностью при хранении. Они применяются для получения резольных смол, прес-материалов и пропитки пористых наполнителей таких как древесина или гипс [2].
Для получения фенолоспиртов применяют реактор такого же типа, что и в производстве фенолоформальдегидных смол периодическим способом (см. рис. 4), в который загружают 37 %-й водный раствор, в котором соотношение формальдегид : фенол составляет 1,15 : 1 и выше [2, 9]. После растворения фенола в реактор добавляют концентрированный водный раствор NaOH из расчета 1,5 мас.ч. на 100 мас.ч. фенола [2]. Полученную реакционную смесь нагревают до 40 оС при помощи подачи пара в рубашку реактора. Затем смесь нагревается за счет теплового эффекта реакции. Путем подачи в рубашку реактора охлаждающей воды выдерживают температуру смеси в пределах 50 – 70°С в течении 5– 12 часов. Готовность фенолоспиртов определяют по содержанию свободного фенола (9–15 % в конце процесса [2]) или свободного формальдегида. По окончанию процесса раствор фенолоспиртов охлаждают до 30 °С и переливают в алюминиевые бочки или бидоны.
Фенолформальдегидный концентрат также упрощает условия транспортировки и хранения обычными резольными смолами, так как не застывает в обычных условиях и не дает осадка параформа. На его основе получают резольные смолы и пресс-материалы, по качеству не уступающие обычным резольным смолам и пресс-материалам, получаемым из них. При этом содержание воды в концентрате на 15–20 % ниже, чем при использовании 37 %-го водного раствора формальдегида и фенола [1, 2].
Заключение
Из представленных в работе сведений следует, что ФФС отличаются большим разнообразием свойств, являясь термопластичными или термореактивными и изначально могут находиться в жидком или твердом состояниях. ФФС хорошо совмещаются с большинством полимеров, что открывает широкие возможности по получению материала, сочетающего преимущества нескольких полимеров.
Это во многом объясняет распространенность фенолформальдегидных пластмасс (фенопластов), представляющих собой композиционные материалы на основе ФФС с различными наполнителями. Благодаря своим прочностным и электроизоляционным свойствам, а также возможностью эксплуатации при высоких температурах и в любых климатических условиях, фенополасты успешно применяются для изготовления конструкционных, фрикционных и антифрикционных изделий, корпусов и деталей электротехнических приборов, для получения строительных материалов и изделий (в том числе во вспененном состоянии), а также в других отраслях промышленности, заменяя сталь, стекло и другие материалы.
Сырьевые материалы для получения ФФС и композиций на их основе являются широко распространенными, а технологии производства относительно не сложными, что позволяет получать их в больших объемах. Главным недостатком ФФС и композиций на их основе, ограничивающим их применение является их сравнительно высокая токсичность. Однако производство и применение ФФС и композиций на их основе остается актуальным и сегодня в связи с востребованностью этого материала, которую можно объяснить не только его эксплуатационными свойствами, но и сравнительно невысокой себестоимостью, износостойкостью и долговечностью.
Библиографическая ссылка
Виткалова И.А., Торлова А.С., Пикалов Е.С. ТЕХНОЛОГИИ ПОЛУЧЕНИЯ И СВОЙСТВА ФЕНОЛФОРМАЛЬДЕГИДНЫХ СМОЛ И КОМПОЗИЦИЙ НА ИХ ОСНОВЕ // Научное обозрение. Технические науки. 2017. № 2. С. 15-28;URL: https://science-engineering.ru/ru/article/view?id=1156 (дата обращения: 25.05.2026).


 science-review.ru
science-review.ru